創新無人區生死看淡
新年的第一記耳光來得比往年更早。
今日,避險資產長江電力、中國神華逆流而上,國資加持的血制品、進可攻退可平替的首仿藥企相對堅挺。
但生活不止眼前的苟活,還需要創新者的冒險精神。2024年創新藥領域最大的突破事件有望在3月14日發生,NASH(非酒精性脂肪肝炎)是當今全世界最大的未滿足需求之一,至今尚無公認有效的藥物獲批上市。在院內感染疫苗、RDN治療領域也存在無人區,等待中國企業破冰。
雖然創新面臨的激勵與風險不平衡,世界總要前進,生死看淡,不服就幹。
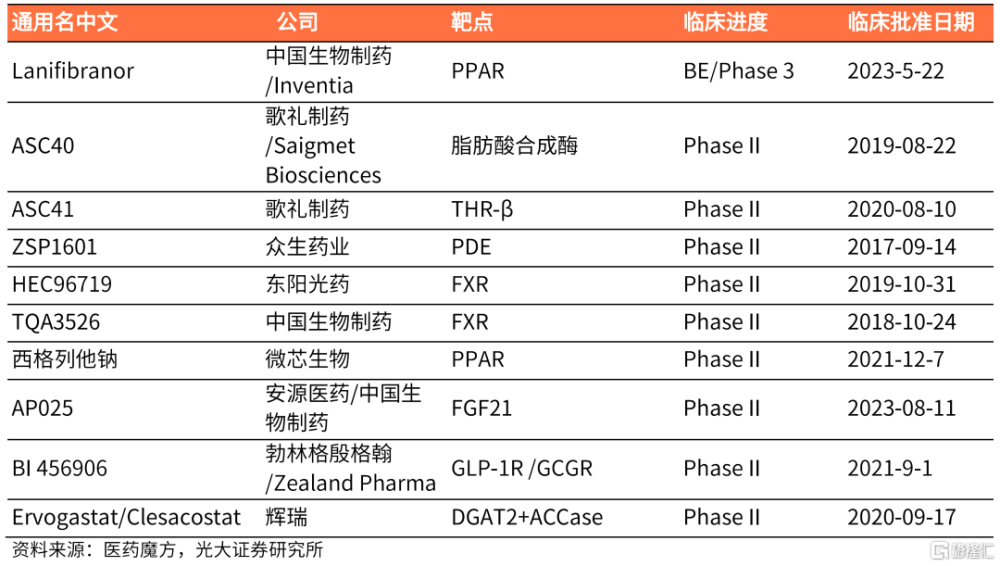 中國NASH在研藥物(II、III 期)
中國NASH在研藥物(II、III 期)
01
2024年創新藥最大突破
當GLP-1減肥藥廣泛衝擊超市、食品、飲料、健身房的景氣度時,還出現過把NASH市場幹沒了的擔憂。
禮來GLP-1三靶點臨牀II期數據顯示用藥48周,患者肝髒脂肪降低率達86%,默沙東GLP-1雙靶點用藥24周肝髒脂肪水平降低72.7%,但肝髒減脂與NASH治療不能劃等號。
NASH的危害在於患者肝纖維化速度較快,平均每個階段的進程爲7年,直至肝硬化或肝癌。NASH 治療需要同時緩解纖維化並降低肝脂肪含量。在一項採用司美格魯肽治療NASH相關肝硬化患者的臨牀II期中,用藥48周,治療組血液指標、脂肪肝變性、體重得到改善,但並未改善NASH症狀或者肝纖維化。
Madrigal研發的甲狀腺激素受體(THR)-β激動劑Resmetirom有望成爲第一個FDA 批准的NASH治療藥物,PDUFA日期爲2024年3月14日。甲狀腺激素通過激活肝細胞中的β受體,在肝功能中發揮核心作用,影響從血清膽固醇和甘油三酯水平,到肝髒中脂肪病理性積聚一系列健康參數。在III期MAESTRO-NASH試驗中,絕大多數(>70%)接受100 mg Resmetirom治療的患者達成≥30%的質子密度脂肪分數(MRI-PDFF)緩解,這與NASH緩解(96%的患者)和纖維化改善(88%的患者)密切相關。
THR-β激動劑 Resmetirom可能不是療效最好的NASH藥物,但最快最穩。進度第二的THR-β激動劑VK2809在2023 年5月達到主要終點,驗證THR-β作爲 NASH治療靶點的成藥性。Akero 的 FGF21 類似物Efruxifermin在NASH引起的代償性肝硬化(F4)患者中暫時遇挫,但逆轉中重度肝纖維化的能力比Resmetirom更強。Inventiva 的PPAR激動劑Lanifibranor完成臨牀II期試驗,展現出比 Resmetirom 更好的纖維化改善能力及更大程度的肝脂肪含量降低。
NASH藥物的競爭,利好賣鏟子的。全球遭受非酒精性脂肪肝病(NAFLD)/NASH 的人群約佔總人口的1/4,患者基數龐大。現有 NAFLD/NASH 檢測的金標准是肝穿刺活檢,存在生理損傷、精度有限的缺點。福瑞股份產品Fibroscan有望成爲下一代無創 NASH 檢測的金標准,基於瞬時彈性成像技術可以高精度定性定量判斷患者肝部脂肪含量與纖維化程度,費用低於核磁共振,設備投放+診斷收費分成的商業模式初步驗證成功。中國生物制藥以1200萬美元首付款從Inventiva引進的 PPAR 激動劑Lanifibranor在國內進度最快,已推進至臨牀III期。歌禮制藥的THR-β激動劑ASC41是可以室溫保存的片劑(競爭對手VK2809是需冷藏保存的膠囊),處於II臨牀試驗。衆生藥業的PDE 抑制劑 ZSP1601,作爲一種全新機理化合物進入臨牀IIb期。
02
中國企業填補世界空白?
全球尚無金葡菌疫苗、銅綠假單胞菌疫苗獲批上市。
院內感染疫苗等待破冰者。據《我國醫院感染管理的現狀及展望》,中國地區醫院感染的發生率爲 1.6%~3.9%,以2021 年住院人數估算,我國總體院內感染人數約爲121.18-295.38 萬人。血液科、重症醫學科、神經外科、骨科、心胸外科、呼吸、結核、感染科是耐藥菌感染高發科室,主要包括金黃色葡萄球菌感染、銅綠假單胞菌感染。耐藥性導致現有抗生素治療方案效果不佳,預防性疫苗是控制傳播的有效手段。
金黃色葡萄球菌可導致患者化膿性關節炎、骨髓炎、膿毒血症、急性肺炎、心內膜炎等嚴重感染並發症。隨着抗生素大量使用,多重耐藥性金黃色葡萄球菌引起嚴重院內感染,平均檢出率30%左右。萬古黴素是治療耐藥性細菌感染的最後一道防线,但糟糕的是,萬古黴素耐藥性金黃色葡萄球菌也已在許多國家分離出來。跨國藥企默沙東、輝瑞、諾華、GSK 的金葡菌疫苗先後進入臨牀研究,其中 3 款已終止,整體未取得顯著進展。
銅綠假單胞菌是一種具有極高致病性及耐藥性的院感細菌, 被WHO列爲“最危級別”的超級耐藥細菌之一,可導致重症肺炎、心內膜炎、胃腸炎、骨髓炎,若未有效控制,將發展爲全身性感染甚至敗血症,死亡率超過60%。上世紀起至少有 60 種在研疫苗,靶點包括脂多糖、胞外多糖、鞭毛、外膜蛋白、細菌毒素、外膜囊泡,最終僅有7種進入臨牀試驗,3 種進入Ⅲ期臨牀,但均宣告失敗。
在這種悲情的氛圍下,歐林生物成爲孤勇者,在國內唯一开展重組金葡菌疫苗臨牀試驗,採用多價+多劑次+佐劑優化抗原和免疫程序設計,當前處於臨牀III期。今年10月,歐林生物從鄒全明教授團隊引進銅綠假單胞菌疫苗原創項目,已啓動人體臨牀試驗程序的申報。
完成跨國藥企未完成之事,填補世界空白有這么容易嗎?在2023年11月的Ⅲ期臨牀試驗期中分析中,DSMB建議歐林生物繼續推進金葡菌疫苗Ⅲ期臨牀研究,但股價一路重挫。
金葡菌疫苗生死未卜,成則收獲國內巨大增量市場、海外巨額BD首付款,敗則一蹶不振。
03
降壓大單品,誰先破局?
醫療器械沉悶的創新氣氛被打破,2023年末迎來一項重磅新興療法,美敦力RDN(腎動脈消融治療)Symplicity Spyral獲得FDA批准上市。
2023年中國頑固型高血壓人群5200萬人,這部分患者很難通過藥物治療達到血壓降低的目的,RDN潛力巨大,國內尚無產品獲批。
研究表明高血壓難以控制的原因之一可能是腎動脈遍布的交感神經過度興奮,RDN微創手術通過介入治療方法,將治療器械臨時置入腎動脈內,發射射頻能量,對腎動脈交感神經進行消融,以減少腦部與腎髒之間的信號傳導,從而幫助控制血壓。
RDN臨牀獲益顯著,可持續降低收縮壓長達三年,在消融完成後取出消融導管,不會留下植入物,不良事件發生率低於1%,沒有出現腎功能損傷。
國內哪家率先闖入這一無人區?
百心安第二代RDN系統Iberis於2023年4月達到主要臨牀終點,並於2023Q2提交注冊申請,爲國內進展最快的RDN廠商之一。Iberis 爲全球唯一可提供兩種介入方式的腎動脈消融產品,且具備較細的導管鞘尺寸。
微電生理RDN系統是一款包含腎動脈射頻消融導管和多路腎動脈射頻消融儀的創新產品,可與電生理三維系統聯用,實現精准定位與消融手術,減少 X 射线對術者和患者的傷害,提升手術的成功率。
康灃生物RDN產品走的是冷凍消融技術路线,研發出全球首款治療高血壓的冷凍消融系統Cryofocus,具有神經損傷完全、消融位置精確、血管內皮損傷小、不易形成血栓的優勢。
不過,美敦力 Symplicity Spyral研發歷時14年,先後遭遇融資困難、更換適應症、臨牀試驗失敗、FDA顧問小組否決的挫折。RDN療法在產品設計、臨牀試驗設計上有着較高難度。美敦力SPYRALHTN全球臨牀項目是研究RDN最全面的臨牀試驗項目,在全球範圍內納入近25000多名患者,以豐富的臨牀數據充分驗證RDN手術治療高血壓的有效性。百心安第二代RDN系統的隨機對照臨牀試驗(Iberis-HTN),共有217名受試者入組。
小企業挑战創新大單品能否成功,今年見分曉。
標題:創新無人區生死看淡
地址:https://www.iknowplus.com/post/68100.html







