集採,息怒
集採七年之癢,是時候作出改變了。
這段時間,湧入小紅書的不僅有TikTok難民,還有用藥群衆,一條熱評吐槽:
“集採藥大家還可以用身體硬抗一波,集採的醫療器械才恐怖呢。”
薛定諤的集採藥。醫生、患者情緒激烈,但身邊統計學不足爲憑據,無法拿出真實世界等效數據,醫保部門卻掌握對自己有利的數據。
國家醫保局2024年12月介紹,前五批國家集採已有63種藥品經過臨牀真實世界研究,全國近百家三級甲等醫院參與,患者樣本量超30萬人,研究結果均顯示仿制藥與原研藥等效。
如果沒有3分錢阿司匹林,本來還歲月靜好。
集採藥頻上熱搜,說明這正是老百姓關切所在,集採爲何費力不討好,值得深思。
2018年“4+7”仿制藥集採至今,已至第十批。高值耗材方面,冠脈支架、骨科(關節、創傷、脊柱)、人工晶體、電生理、IVD(生化、化學發光)都經歷集採。
羅馬不是一天建成的,集採七年,仍有需要完善之處。不汲取教訓,說不定又會有什么藥或械引爆全民情緒。
讓我們從爭吵的紛擾中脫離出來,回到平靜理性軌道,能否從一些基礎性建設工作做起?
01
提高仿制藥一致性評價標准
上海臨牀一线醫生喜歡當吹哨人。
去年1月,也是上海兩會期間,復旦大學附屬中山醫院麻醉科主任繆長虹建議,藥品一致性評價指標和過評仿制藥質量保障有待完善。“一致性評價主要採用生物等效性的標准,諸如質量標准、藥物活性成分的晶型和粒度、雜質等主要藥學指標以及不良反應等目前暫未納入一致性評價。”
早在2023年2月,梅斯醫學平台上一篇文章《原研VS 仿制 “一致“是否等於”一樣“?》也提到類似觀點。
目前,國內仿制藥一致性評價僅要求評估藥學等效和生物等效,因此,僅是通過一致性評價,並不能完全代表臨牀等效。
1、評價指標的局限性:決定仿制藥與原研藥質量差異的因素有藥品的藥學特性、輔料、生產工藝、雜質、穩定性和溶出度等。藥學等效性研究中未涵蓋質量標准、藥物活性成分的晶型和粒度、雜質等主要藥學指標的一致性比較。即使是同一藥物,如果粒度或晶型不同,不僅物理性質會有所不同,其生物活性也有明顯差異,臨牀應用受到幹擾。相似的,即使輔料的品種和型號相同,加入的量和順序上的差異最終影響藥品的臨牀療效。而輔料的控制、工藝、生產是我國制藥業的薄弱環節[1] 。
2、生物等效性研究局限性:因時間、樣本量以及健康受試者和患者生理狀況的差異,單劑量研究難以反映長期用藥的實際情況[2]。比如出於倫理和研究考慮,BE試驗大多是在18-40周歲、18-24例健康受試者身上所進行的,而藥品上市後使用中對象多爲老人及疾病患者,藥物在兩種不同人群體內的代謝情況將有較大差別。另外用於生物等效判定的重要參數值僅爲區間要求,存在非完全等效的可能性,導致療效或不良反應上的差異[3]。
一致性評價缺乏長期穩定性和批間質量差異的驗證,隨時間變化和不同批次引起的質量穩定性差異最終體現在藥品的療效和安全性上。21項RCT研究的Meta分析結果顯示,在有效性方面,原研藥與仿制藥在降低患者LDL-C 和升高 HDL-C 的程度方面差異無統計學意義,而在降低患者TC、TG的程度方面,仿制藥小於原研藥,並且差異有統計學意義[4]。
一項通過對比原研與仿制莫西沙星注射液在治療社區獲得性肺炎中的成本-效果分析,發現仿制和原研的7d有效率接近,原研藥雖略高但無統計學差異。然而在不良反應發生率方面,仿制組顯著高於原研組[5]。
一項研究結合北京市集採中選的25個藥品採購、臨牀診療及不良反應數據,對集採中選藥品使用情況及效果予以分析,藥品不良反應觀察時間爲:2017年3月23日至2021年3月22日。研究結果顯示,有一半以上的藥品在帶量採購後ADR上報率有所增加,其中厄貝沙坦的不良反應上報率達到帶量前的2.5倍[6]。
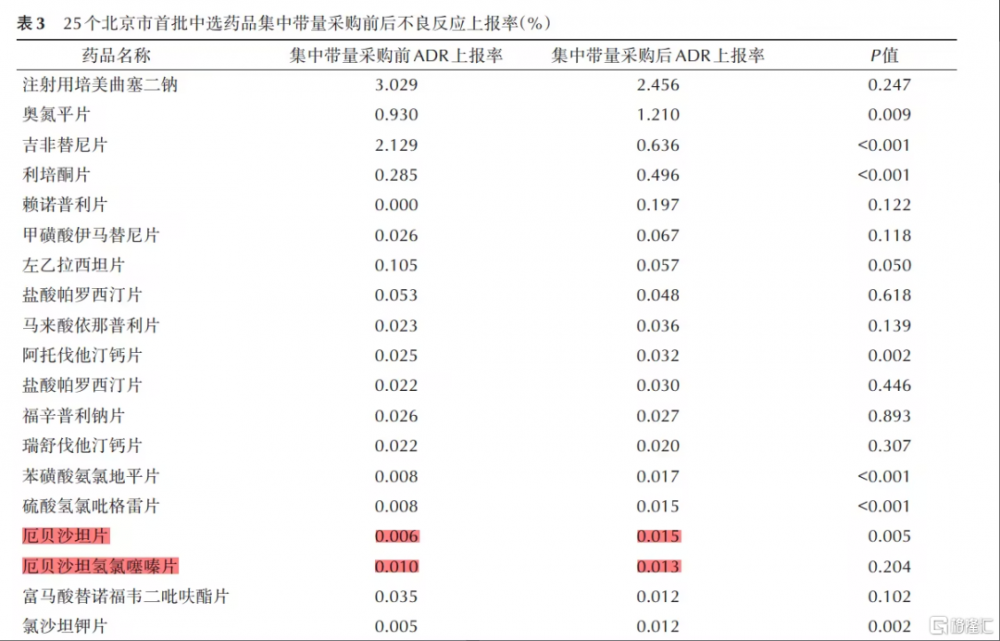
提高仿制藥一致性評價標准,勢必將增加成本,這需要集採定價時爲藥企預留合理的利潤空間。
3分錢阿司匹林,收回物料成本容易,但一致性評價成本也不容忽視。2020年第三批國家集採結束後,醫藥魔方根據上市公司公告,統計了44個中選藥品的一致性評價研發(包含視同通過)費用,共計4.87億元,每個藥品平均1107萬元。若不考慮其既往收入,只以此次中標價格來看,有8個藥品至少需要賣出1億片(按主規格計)以上才能收回成本。其中,恩華藥業的氯氮平片以0.016元/片的價格中選,按其公告的668萬元一致性評價費用來算,需要賣出42278萬片才能收回成本,大約爲422.78萬盒(規格包裝25mg*100片)。
氯氮平片主要用於治療精神分裂症、躁狂症。
02
避免無底线低價中標
集採殘酷性,是由行業內卷局面決定的。
國家醫保局在1月17日的發布會上表示,“希望競爭激烈度保持在合理範圍,但這需要行業自身走到差異化發展道路上,主動避免在同一種成分、同一個靶點上過度重復立項,避免加劇供大於求,醫保部門愿意看到一個藥物由適量的企業生產,希望產能和需求基本匹配,不愿看到37家甚至50家企業同時生產一種藥物,產能數十倍、數百倍於需求,這種情況下,市場競爭的壓力必將把價格拖到谷底。”
誰該死,誰該活,應該交給市場自行出清。集採的正確性在於低價與藥效的平衡,擠出藥耗價格虛高水分,減輕用藥群衆負擔。在規則設計上應避免囚徒困境,丟標企業固然不值得同情,中標企業也要確保收回成本。
復盤第十批國採,巨大爭議的源頭是一條規則之變。
取消降價≥50%即可中選的兜底規則,改爲不高於同品種最低“單位可比價”1.8 倍可中選,這加劇藥企的囚徒困境博弈,因爲不知道對手出價是多少,萬一對手出價超低,自己可能直接失去入圍資格。
於是,國採現場譁然,驚嘆聲此起彼伏,平均降價幅度創下歷史之最。據醫藥魔方統計,從產品實際降幅(vs省份最低價)來看,大部分降幅都集中在90%以上,爲了獲取中選資格和順位競爭激烈。
令人欣慰的是,去年12月底,安徽28省IVD集採規則回歸溫和,降幅>50%即可確保中標,因此,A組大多數企業報出50.01%的降幅,最高降幅不超過50.2%。
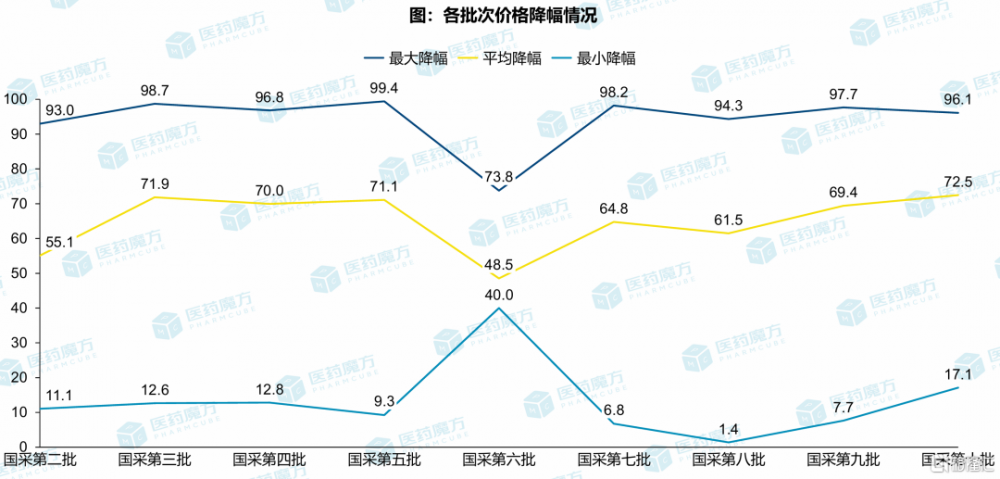 第十批國採涉及品種的最高申報價普遍較低,所以從最高申報價降幅看,第十批價格降幅較以往化藥批次整體平均降幅有所升高 數據來源:醫藥魔方PharmaGO®數據庫-中標庫 數據解釋:未換算規格/包裝差比價
第十批國採涉及品種的最高申報價普遍較低,所以從最高申報價降幅看,第十批價格降幅較以往化藥批次整體平均降幅有所升高 數據來源:醫藥魔方PharmaGO®數據庫-中標庫 數據解釋:未換算規格/包裝差比價
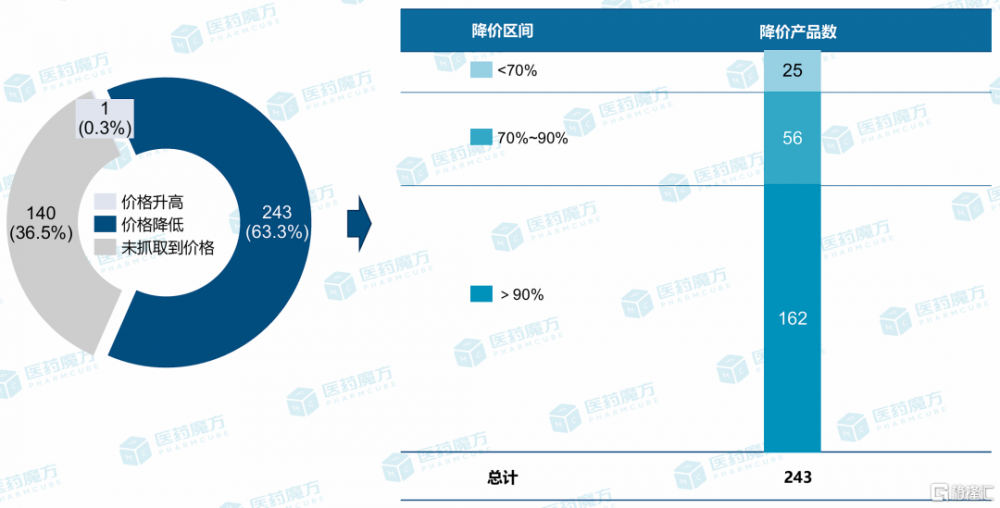 數據來源:醫藥魔方PharmaGO®數據庫-中標庫 數據解釋:換算規格/包裝差比價
數據來源:醫藥魔方PharmaGO®數據庫-中標庫 數據解釋:換算規格/包裝差比價
03
建立集採藥不良反應報告制度
這不難。
集採藥沒有臨牀藥物不良反應的監測報告,但原研藥每個月都有。
上海政協委員、瑞金醫院普外科主任鄭民華建議,“鼓勵臨牀醫生和患者向國家不良反應監測中心報告藥品不良反應和藥品療效缺陷。藥品療效存在疑問,是對患者最大的安全隱患,更應該及時報告。”
建立統一的反饋通路,合規收集真實世界數據,可避免醫生、患者的碎片化個體感受缺乏權威性。
集採中標只是起點,需要全程動態監控,民革上海市委建議,對於獲得一致性認證的藥品在進入集採環節後,要定期或不定期對藥廠進行藥品檢測,直接從醫院抽查藥品,確保抽樣藥物和一致性認證過程中的各項藥效完全相同。
04
不宜再渲染靈魂砍價
每年醫保談判後,都會播出靈魂砍價的視頻。
其實,這種導向已經不合時宜,與社會主要關切脫節了。相比降價,用藥群衆現在更關心藥效。
老百姓從最初感動抹淚,到現在認識到“一分錢一分貨”的道理,所謂價廉物美是要講良心的,而良心這玩意兒不靠譜。在網絡平台上,部分慢病患者甚至認識到藥企也是有生產成本、研發成本的。
集採、醫保談判在降價上已經做得夠好了,沒人還會懷疑控費力度不夠,現在應該向公衆傳遞國產藥全鏈條在保證藥效上所做的努力。
醫藥是一個超級龐雜的系統,生產方是企業,定價和支付方是醫保,決策方是醫生,需求方是患者,常規市場經濟的幾個要素在此是割裂的,而且醫藥兼備民生保障屬性、科技創新屬性,不能完全交給市場去調節,但政策端在協調效率與公平上也面臨挑战。
醫藥產業鏈各方利益、各種因素互相影響,牽一發而動全身,可能存在結果與過程相違、整體與局部相悖的情況。集採協議量一般在醫療機構報量的60%-80%,剩余部分由醫療機構自主選擇擬採購品牌,確實沒有限制採購使用“進口原研藥”,但是,因爲面臨或明或暗的規則(掛網銷售條件、集採用量考核、DRG考核、自費率考核),有的醫院爲管理方便,一刀切只進集採藥,造成進口原研藥不好开的現狀。就像之前引起關注的“15天強制出院”爭議,醫保部門說從來沒有15天強制出院的規定,但是因爲單病種付費、DRGs付費辦法,醫保基金對單個病人單次治療的報銷費用有總額限制,用完限額病還沒好,醫院只能讓病人出院再重新入院。
面對這個錯綜復雜的醫藥系統,我們要保持敬畏之心。千頭萬緒,患者的臨牀需求至爲重要。
標題:集採,息怒
地址:https://www.iknowplus.com/post/187374.html







