2023年諾貝爾生理學或醫學獎揭曉!兩位mRNA技術开創者獲獎
北京時間10月2日下午,2023年諾貝爾生理學或醫學獎揭曉!
瑞典卡羅林斯卡醫學院諾貝爾獎委員會宣布,卡塔琳·考裏科(Katalin Karikó) 和 德魯·韋斯曼(Drew Weissman)榮膺2023年諾貝爾生理學或醫學獎,以表彰他們在核苷鹼基修飾方面的發現,這些發現使得針對COVID-19的有效mRNA疫苗得以开發,他們將共享1100萬瑞典克朗獎金(約合732萬元人民幣)。

諾貝爾官方新聞稿表示,這兩位諾貝爾獎獲得者的發現對於在2020年初开始的新冠肺炎大流行期間开發有效的mRNA疫苗至關重要。通過他們的突破性發現,從根本上改變了人們對信使核糖核酸如何與免疫系統相互作用的理解,獲獎者爲疫苗开發的空前速度做出了貢獻。
諾獎官網對Katalin Karikó 和 Drew Weissman 的研究成果介紹如下:
疫情爆發前的疫苗
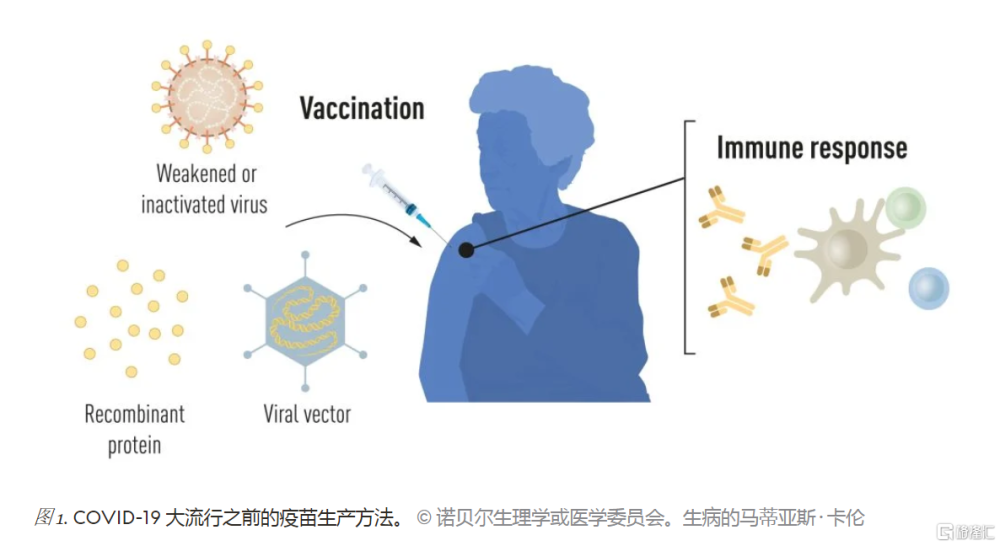
疫苗接種會刺激針對特定病原體的免疫反應的形成。這使得身體在以後接觸疾病時能夠搶佔先機。基於滅活或弱化病毒的疫苗早已問世,例如針對脊髓灰質炎、麻疹和黃熱病的疫苗。1951 年,Max Theiler 因研制出黃熱病疫苗而獲得諾貝爾生理學或醫學獎。
由於近幾十年來分子生物學的進步,基於單個病毒成分而不是整個病毒的疫苗已經被开發出來。部分病毒遺傳密碼通常編碼病毒表面的蛋白質,用於制造刺激病毒阻斷抗體形成的蛋白質。例如針對乙型肝炎病毒和人乳頭瘤病毒的疫苗。或者,部分病毒遺傳密碼可以轉移到無害的攜帶病毒中,即“載體”。該方法用於抗埃博拉病毒的疫苗。當注射載體疫苗時,選定的病毒蛋白會在我們的細胞中產生,刺激針對目標病毒的免疫反應。
生產基於病毒、蛋白質和載體的疫苗需要大規模細胞培養。這種資源密集型過程限制了快速生產疫苗以應對疫情和大流行的可能性。因此,研究人員長期以來一直試圖开發獨立於細胞培養的疫苗技術,但這被證明具有挑战性。
mRNA 疫苗:一個有前景的想法
在我們的細胞中,DNA 中編碼的遺傳信息被轉錄成信使 RNA (mRNA),mRNA 是蛋白質產生的模板。20 世紀 80 年代提出了一種了無需細胞培養即可產生 mRNA 的有效方法,即體外轉錄。這決定性的一步加速了分子生物學在多個領域應用的發展。將 mRNA 技術用於疫苗和治療目的的想法也开始興起,但前路上仍有障礙。
體外轉錄的 mRNA 不穩定且難以傳遞,需要开發復雜的載體脂質系統來封裝 mRNA。此外,體外產生的 mRNA 會引起炎症反應。因此,开發用於臨牀的 mRNA 技術的熱情最初非常有限。
這些障礙並沒有讓匈牙利生物化學家 Katalin Karikó 灰心,她致力於开發利用 mRNA 療法。20 世紀 90 年代初,她在賓夕法尼亞大學擔任助理教授,盡管在很難說服研究資助者她的項目具有重大意義,但她始終堅持自己的理想,即實現 mRNA 療法。
Karikó 在大學裏的一位新同事是免疫學家 Drew Weissman。他對樹突狀細胞感興趣,而樹突狀細胞在免疫監視和激活疫苗誘導的免疫反應中具有重要功能。在新想法的推動下,兩人很快开始了合作,重點研究不同 RNA 類型如何與免疫系統相互作用。
突破
Karikó 和 Weissman 注意到,樹突細胞會把於體外環境轉錄的 mRNA 識別爲外源物質,進而導致樹突細胞的激活和炎症信號因子的釋放。他們驚訝於爲何體外環境轉錄的 mRNA 會被樹突細胞識別,而哺乳動物細胞轉錄的 mRNA 則並不會引發同樣的反應。Karikó 和 Weissman 意識到,樹突細胞一定是靠某些重要特徵區分了不同類型的 mRNA。
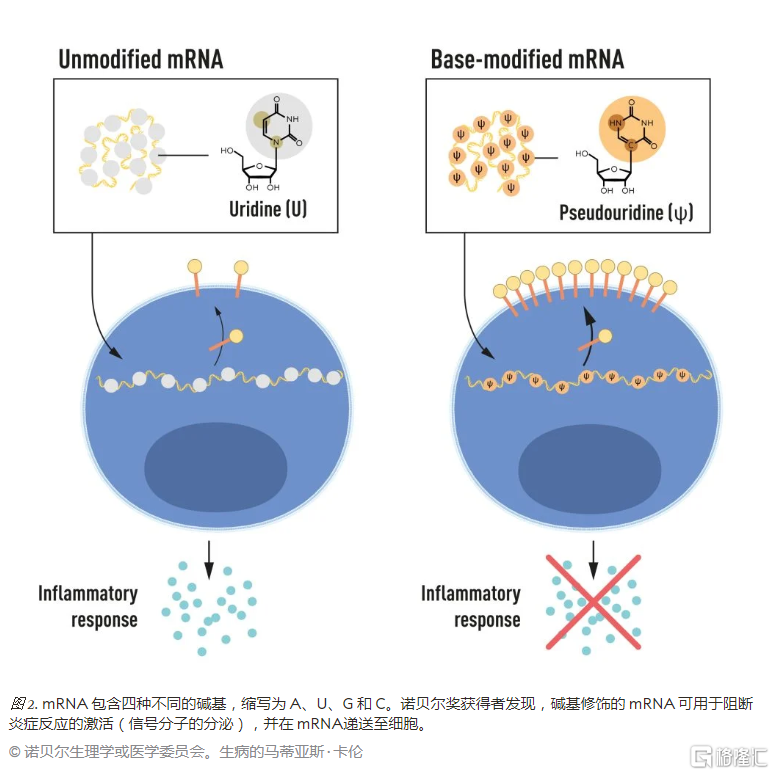
RNA 由四種縮寫爲 A、U、C、G 的鹼基所構成,相應地,遺傳密碼的載體 DNA 由四種縮寫爲 A、T、C、G 的鹼基所構成。Karikó 和 Weissman 知道,哺乳動物細胞中的 RNA 核苷酸鹼基常存在化學修飾,而體外環境轉錄的 mRNA 並非如此。他們還驚詫於體外環境轉錄的 mRNA 中鹼基修飾的缺失可以解釋非預期炎症反應的發生。
爲了研究這一點,他們合成了多種不同的 mRNA,每種都在鹼基上有獨特的修飾,並將這些 mRNA 輸送至樹突細胞中。研究結果令人震驚:當 mRNA 中引入鹼基修飾時,炎症反應幾乎消失。這改變了我們對細胞識別和響應不同種類的 mRNA 的典型認知。
Karikó 和 Weissman 很快意識到他們的發現將會對 mRNA 療法產生重大影響,他們這一具重大意義的研究成果於 2005 年,也就是新冠病毒流行的 15 年前發表。
在 2008 年和 2010 年發布的後續研究中,Karikó 和 Weissman 闡明了相比未修飾的 mRNA,鹼基修飾後的 mRNA 可以顯著增加蛋白合成。這一效應可歸結於調節蛋白質合成的酶的激活減少。通過這些發現,即鹼基修飾可以同時降低炎症反應和增加蛋白質合成,Karikó 和 Weissman 根除了 mRNA 臨牀應用中的關鍵障礙。
mRNA 疫苗發揮了其潛力
人們對 mRNA 技術的興趣开始升溫,2010 年,多家公司开始致力於开發該方法。研發針對寨卡病毒和中東呼吸綜合徵冠狀病毒的疫苗;後者與SARS-CoV-2密切相關。COVID-19 大流行爆發後,兩種編碼 SARS-CoV-2 表面蛋白的鹼基修飾 mRNA 疫苗以創紀錄的速度开發出來。據報道,保護效果約爲 95%,這兩種疫苗早在 2020 年 12 月就獲得了批准。
mRNA 疫苗的开發具有令人印象深刻的靈活性和速度,爲使用新平台开發針對其他傳染病的疫苗鋪平了道路。未來,該技術還可用於輸送治療性蛋白質並治療某些癌症類型。
基於不同方法的其他幾種針對 SARS-CoV-2 的疫苗也迅速推出,全球總共已接種超過 130 億劑 COVID-19 疫苗。這些疫苗挽救了數百萬人的生命,並預防了更多人的嚴重疾病,使社會得以开放並恢復正常狀態。今年的諾貝爾獎獲得者通過對 mRNA 鹼基修飾重要性的基本發現,在我們這個時代最大的健康危機之一期間爲這一變革性發展做出了重要貢獻。
關於Katalin Karikó和Drew Weissman
卡塔林·卡裏科(Katalin Karikó), 卡塔林·卡裏科1955年出生於匈牙利紹爾諾克。
她出生自一個匈牙利小鎮,20多歲遷居美國,其求學經歷非常勵志,但幾十年都沒有固定職位,一直遊走於學術界邊緣。
1982年,她從塞格德大學獲得博士學位,並在塞格德的匈牙利科學院進行博士後研究,直到1985年。
隨後,她在費城坦普爾大學和貝塞斯達健康科學大學進行了博士後研究。
1989年,她被任命爲賓夕法尼亞大學助理教授,一直任職到2013年。之後,她成爲BioNTech RNA Pharmaceuticals的副總裁,後來成爲高級副總裁。
自2021年以來,她一直是塞格德大學的教授和賓夕法尼亞大學佩雷爾曼醫學院的兼職教授。
在獲得2023年諾貝爾生理學或醫學獎之前,Katalin Karikó與獲得2022年科學突破獎之生命科學獎、2021年拉斯克臨牀醫學研究獎、2022年度“世界傑出女科學家獎”等獎項。

值得一提的是,在此前諾貝爾生理學或醫學獎的獲獎者中,包含了12位女性,最近一次獲得該獎項的女科學家是屠呦呦,而Katalin Karikó將成爲第13位榮獲該殊榮的女科學家。
而Drew Weissman博士同樣是賓夕法尼亞大學科學家,他與Katalin Karikó共同獲得了2022年科學突破獎之生命科學獎以及拉斯克臨牀醫學研究獎。
德魯 · 魏斯曼(Drew Weissman), 1959年出生於美國馬薩諸塞州的列克星敦。
1987年,他在波士頓大學獲得了博士學位和博士學位。他在哈佛醫學院貝斯以色列女執事醫療中心進行臨牀培訓,在國立衛生研究院進行博士後研究。
1997年,韋斯曼在醫學佩雷爾曼學院賓夕法尼亞大學成立了自己的研究小組。他是羅伯茨家庭疫苗研究教授和賓夕法尼亞大學 RNA 創新研究所所長。

還有這些獎項將逐次揭曉
10月3日——物理學獎 歐洲中部時間11時45分(北京時間17時45分)
10月4日——化學獎 歐洲中部時間11時45分(北京時間17時45分)
10月5日——文學獎 歐洲中部時間13時(北京時間19時)
10月6日——和平獎 歐洲中部時間11時(北京時間17時)
10月9日——經濟學獎 歐洲中部時間11時45分(北京時間17時45分)
標題:2023年諾貝爾生理學或醫學獎揭曉!兩位mRNA技術开創者獲獎
地址:https://www.iknowplus.com/post/38236.html







